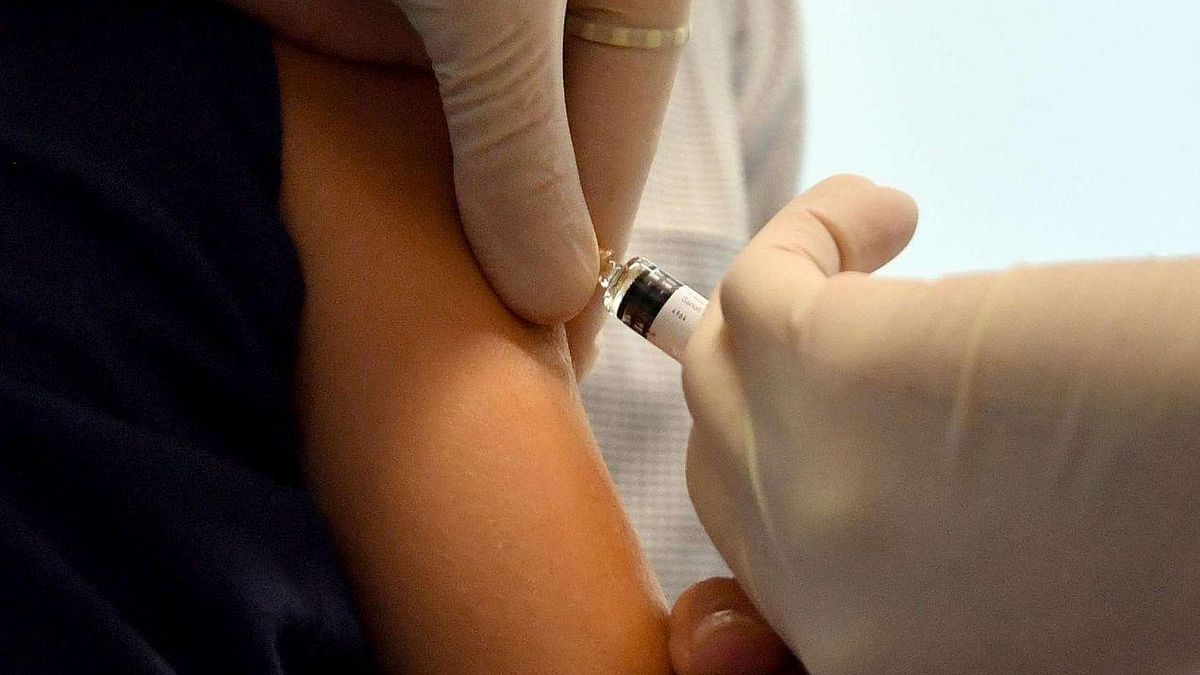
Vaccino anti-coronavirus, AstraZeneca: "Possiamo ancora farcela per il 2020"
L'amministratore delegato Pascal Soriot apre uno spiraglio dopo la sospensione temporanea della sperimentazione
© ansa
Il vaccino sperimentale anti-coronavirus elaborato dall'Università di Oxford potrebbe ancora essere disponibile sul mercato "a fine anno o all'inizio del 2021", malgrado la battuta d'arresto della terza fase di test imposta dalla reazione anomala registrata su un paziente. Lo ha affermato Pascal Soriot, amministratore delegato di AstraZeneca, il colosso farmaceutico che si è aggiudicato i diritti di produzione del vaccino.
Tutto ancora aperto - Soriot ha precisato di non poter dire esattamente quando i trial riprenderanno, ma di essere comunque convinto che il progetto resti "in corsa per avere entro quest'anno una data" sulla richiesta di approvazione da parte delle autorità sanitarie. "Un vaccino potrebbe poi essere disponibile a fine anno o all'inizio del prossimo", a seconda della rapidità dei tempi di approvazione dei regolatori, ha sostenuto il ceo di AstraZeneca.
Gli eventi avversi nei test "sono abituali" - Quanto all'episodio del paziente soggetto a reazione anomala, Soriot ha notato che "eventi avversi" sono abituali nelle fasi di sperimentazione, ma che normalmente "non sono tenuti sotto osservazione dal mondo intero". L'a.d. ha quindi aggiunto che la diagnosi di un'infiammazione spinale sul volontario colpito dal potenziale effetto collaterale non è ancora confermata.
La pronuncia del comitato - I tempi entro i quali il comitato di esperti indipendenti dovrà pronunciarsi, stabilendo se la reazione sospetta sia stata determinata dall'inoculazione del vaccino o meno, "possono variare da una settimana a tre mesi". Lo afferma il presidente di Irbm Piero Di Lorenzo, aggiundendo: "Se la valutazione del comitato sarà positiva, l'azienda riprenderà subito la sperimentazione".