Perché AstraZeneca ha ritirato il suo vaccino contro Covid? Ci sono rischi? La scheda
L'azienda ha ritirato il suo vaccino contro il Covid a livello globale. Prodotto poco richiesto e non più aggiornato rispetto alle varianti. Nessun nesso con gli effetti collaterali già noti
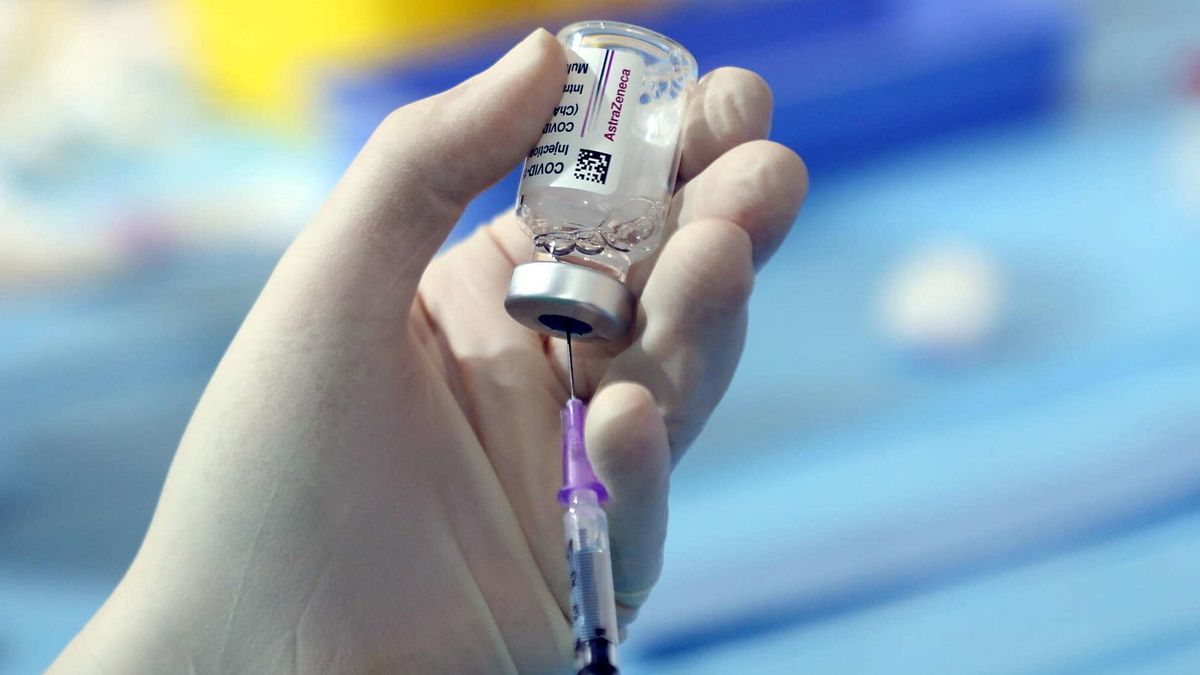
© Ansa
Il 7 maggio il comitato di sicurezza dell’ama (Agenzia europea del farmaco) ha emesso un avviso in cui sconsiglia l’uso del vaccino AstraZeneca Vaxzevria citando un’ampia disponibilità di vaccini più recenti adattati alle varianti del virus. In molti associano la notizia del ritiro al procedimento penale avvenuto a Londra, nel quale l’azienda anglo-svedese ha ammesso che il suo vaccino può causare trombosi come raro effetto collaterale, ma è un nesso privo di fondamento – spiega a Tgcom24 Matteo Bassetti, direttore della clinica di malattie infettive dell'ospedale San Martino di Genova.
“Quello relativo alla trombosi è un fenomeno noto da tempo, tanto che stato inserito nel foglietto illustrativo tra i possibili rari effetti collaterali; infatti nel nostro Paese il vaccino di AstraZeneca non si utilizza più dal 2021. Il prodotto è stato ritirato semplicemente perché si tratta di un vaccino vecchio e non più adeguato rispetto alle varianti. Ed è la ragione per cui l’Ue ha deciso di puntare su quei vaccini a mRna più velocemente adattabili alle nuove varianti”.
Che caratteristiche ha il vaccino Vaxzevria?
Si tratta di un vaccino a vettore virale basato sull'adenovirus ChAdOx1, sviluppato presso lo Jenner Institute dell'Università di Oxford in collaborazione con AstraZeneca e l'italiana IRBM Science Park. Era stato approvato nel Regno Unito il 30 dicembre 2020.
A fine gennaio 2021 anche Ema (Agenzia europea per i medicinali) e poi Aifa (Agenzia italiana del farmaco) aveva dato il via libera alle somministrazioni nei soggetti di 18 anni o più. ChAdOx1è un adenovirus degli scimpanzé (Chimpanzee Adenovirus Oxford 1), responsabile del raffreddore comune. Per produrre il vaccino ne è stata utilizzata una versione indebolita, cioè incapace di replicarsi e innocua per l’organismo umano, nella quale è stato inserito il materiale genetico della proteina Spike di Sars-CoV-2.
Una volta somministrato il vaccino, l’adenovirus penetra nel nucleo della cellula dove fornisce il codice genetico per produrre la proteina Spike. In questo modo le cellule T attivano la risposta immunitaria e la produzione di anticorpi specifici contro il virus.
Per quali categorie è stato utilizzato il vaccino?
A fine gennaio 2021 l'Ema aveva autorizzato Vaxzevria solo per persone al di sotto dei 60 anni, perché non c'erano dati di efficacia e sicurezza sufficienti negli anziani. Poco dopo, a febbraio, era arrivato il via libera anche per gli over 60: a quel punto il vaccino risultava approvato per tutti gli adulti, dai 18 anni in su.
In seguito, ad aprile 2021, erano stati segnalati i primi rari casi di trombocitopenia trombotica. A inizio maggio, dopo le prime evidenze sui casi di trombosi, anche se la correlazione non era ancora sicuramente dimostrata, il Ministero della Salute aveva raccomandato, come misura cautelativa, di riservare il vaccino alle persone dai 60 anni in su.
“I vaccini a base di vettore adenovirale si sono mostrati fin dall’inizio meno efficaci di quelli a mRna- afferma il dottor Sergio Abrignani, professore ordinario di Immunologia e Immunopatologia all’Università Statale di Milano e direttore dell’Istituto nazionale di genetica molecolare Romeo ed Enrica Invernizzi - Se avessimo avuto fin dall’inizio grande disponibilità dei vaccini a mRna probabilmente quelli a vettore virale non sarebbero stati usati. Fin dall'inizio i vaccini a vettore virale hanno anche avuto una limitazione immunologica: non possono essere usati come richiami, perché dopo la seconda dose si sviluppa spesso una risposta immunitaria contro la componente adenovirale, che potrebbe rendere inefficaci le dosi successive”.
Come veniva somministrato il vaccino di AstraZeneca?
Il vaccino Vaxzevria veniva somministrato in due dosi, nel muscolo del braccio: la seconda deve essere somministrata nel corso della dodicesima settimana e comunque a una distanza di almeno dieci settimane dalla prima.
Il problema degli eventi avversi riguarda solo il vaccino di AstraZeneca? No, riguarda tutti i vaccini a vettore virale, quindi anche quello prodotto da Johnson & Johnson/Janssen (Ad26.COV2.S). Dopo il sospetto di un collegamento con i casi di trombocitopenia trombotica, tra marzo e aprile 2021, l’utilizzo del vaccino prodotto da AstraZeneca è stato bloccato dalle autorità sanitarie di diversi Paesi europei e il suo utilizzo è stato successivamente ri-approvato dall’Ema previa valutazione del rapporto rischio/beneficio. I vaccini a mRna non hanno associazioni con il raro rischio di trombocitopenia trombotica.
Chi lo ha ricevuto rischia qualcosa?
“Tranquillizziamo definitivamente tutti quelli che sono stati vaccinati con AstraZeneca – dice a Tgcom24 Matteo Bassetti, direttore della clinica di malattie infettive dell'ospedale San Martino di Genova - tutti i casi segnalati di trombosi indotta da vaccino si sono verificati entro due settimane dalla somministrazione del vaccino, quindi chi ha ricevuto il vaccino AstraZeneca da diversi mesi o addirittura anni non corre rischi di svilupparla”.